TCGA-KIRC mRNA表达与临床数据集分析指南
在生物医学研究领域,The Cancer Genome Atlas (TCGA) 项目是一个标志性的国际研究合作项目,旨在通过全面的基因组分析,揭示肿瘤的分子亚型并识别影响癌症发展的遗传变异。本章将对TCGA项目进行概述,介绍其起源、目标和提供的数据类型。随后,我们将探讨TCGA-KIRC研究的重要性,即针对肾透明细胞癌的研究,以及TCGA-KIRC数据集的构成、结构和使用指南。TCGA项目于20
简介:TCGA是一项国际癌症研究项目,专注于通过基因组和转录组分析提升癌症理解。TCGA-KIRC研究专项针对肾透明细胞癌,提供了标准化mRNA表达数据(TPM格式)及临床信息。数据集可用于分析基因表达变化、寻找疾病相关基因,并结合临床特征探索基因与临床结果之间的关联。数据处理步骤包括清洗、转换、统计分析及生存分析,有助于揭示疾病的分子机制并推动新疗法发展。 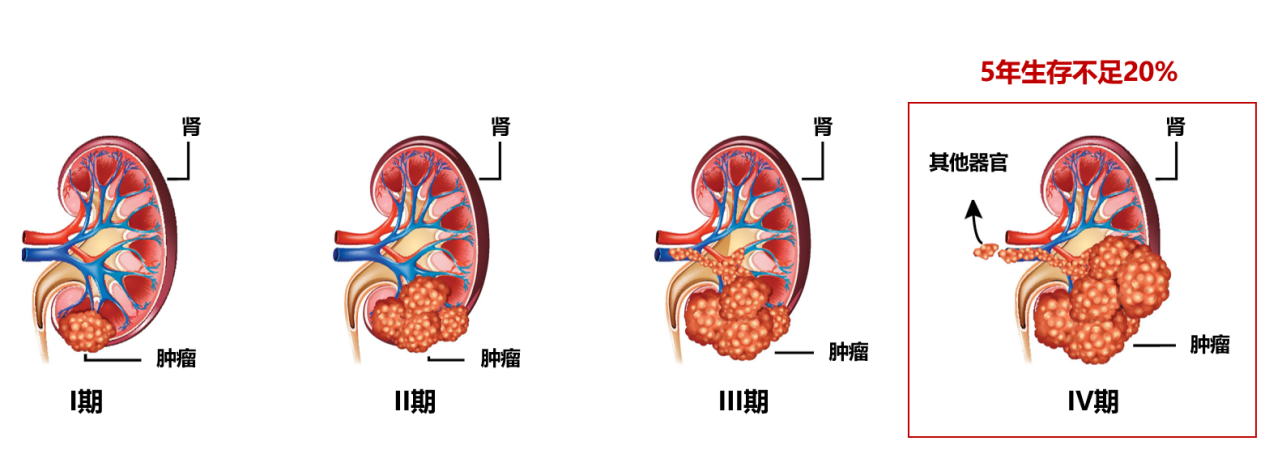
1. TCGA项目和TCGA-KIRC研究介绍
在生物医学研究领域,The Cancer Genome Atlas (TCGA) 项目是一个标志性的国际研究合作项目,旨在通过全面的基因组分析,揭示肿瘤的分子亚型并识别影响癌症发展的遗传变异。本章将对TCGA项目进行概述,介绍其起源、目标和提供的数据类型。随后,我们将探讨TCGA-KIRC研究的重要性,即针对肾透明细胞癌的研究,以及TCGA-KIRC数据集的构成、结构和使用指南。
1.1 TCGA项目概述
1.1.1 TCGA项目的起源和目标
TCGA项目于2006年启动,旨在创建一个全面的癌症基因组数据集合,进而推动癌症治疗的研究。该项目由美国国家癌症研究所(NCI)和国家人类基因组研究所(NHGRI)共同资助。TCGA的目标是系统地绘制多种肿瘤类型的基因图谱,包括体细胞突变、基因组重排、mRNA和miRNA表达,以及DNA甲基化等信息,从而提供深入了解癌症分子基础的资源。
1.1.2 TCGA项目的数据类型和使用
TCGA项目产生的数据类型多样,包括全外显子组测序、全基因组测序、转录组分析、表观遗传学数据等。这些数据可通过TCGA数据门户网站公开获取,供全球研究者使用。数据的使用不仅限于基础研究,还涉及临床应用的探索,如新型生物标志物的发现和癌症精准医疗的开发。
1.2 TCGA-KIRC研究的重要性
1.2.1 肾透明细胞癌的疾病特征
肾透明细胞癌(KIRC)是肾癌中最常见的类型,占肾脏恶性肿瘤的约75%。该癌症的特点是细胞胞质丰富、透明,且常伴随有VHL基因突变。KIRC的侵袭性较强,晚期患者预后较差,因此深入研究其分子机制对于改善临床治疗至关重要。
1.2.2 TCGA-KIRC研究对医学的贡献
TCGA-KIRC研究提供了肾透明细胞癌的全面基因组视图,揭示了肿瘤发生发展的关键遗传和表观遗传变异。研究结果促进了肾癌生物学的理解,为新治疗方法的开发提供了重要线索。同时,研究还促进了基于分子特征的新型预后标志物和治疗靶点的发现。
1.3 TCGA-KIRC数据集的特点
1.3.1 数据集的构成和结构
TCGA-KIRC数据集包含了来自超过500名肾透明细胞癌患者的综合分子谱数据。数据集包括患者的临床信息、基因表达数据、基因组变异数据、表观遗传数据等多个层面。数据集的结构被设计得既便于访问也便于分析,包含有详细的样本元数据和注释信息。
1.3.2 数据集的获取和使用指南
TCGA-KIRC数据集可以通过Genomic Data Commons (GDC) 数据门户或使用GDC Data Transfer Tool下载。在使用这些数据前,研究者需注册并同意数据使用协议。数据的使用指南涵盖从数据检索、下载到处理和分析的全过程,确保研究者可以高效、合规地利用TCGA-KIRC资源。
以上章节为TCGA项目和TCGA-KIRC研究的基本介绍,通过这些内容,读者将对该项目及其在肾透明细胞癌研究中的应用有一个整体的理解。下一章将详细介绍mRNA表达数据的TPM标准化方法及其在数据分析中的重要性。
2. mRNA表达数据的TPM标准化及其重要性
2.1 TPM标准化的基本概念
2.1.1 TPM标准化的定义和原理
TPM(Transcripts Per Kilobase Million)标准化是一种用于mRNA表达分析的规范化方法,旨在使不同样本或组之间的转录本计数具有可比性。通过计算每百万个转录本中的每个基因的转录本计数,TPM标准化能够减少因测序深度不同而引起的样本间的表达差异,从而允许研究人员比较不同实验条件下的基因表达水平。
TPM标准化的数学表达:
TPM的计算可以概括为以下步骤:
- 计算每个基因在其所属样本中的转录本计数占总转录本计数的比例。
- 将此比例乘以10^6,得到TPM值。
具体公式表示为:
[TPM_i = \frac{C_i}{L_i} \times 10^6]
其中,(C_i) 代表基因i在样本中的转录本计数,(L_i) 代表样本中所有基因的总转录本长度的和。
2.1.2 TPM与其他标准化方法的比较
在RNA-Seq数据分析中,除了TPM,还存在诸如FPKM(Fragments Per Kilobase of exon per Million fragments mapped)和RPKM(Reads Per Kilobase of transcript per Million reads mapped)等其他标准化方法。尽管这些方法在原理上与TPM相似,但它们在处理转录本长度和测序深度方面存在差异。
FPKM和RPKM在计算转录本的片段或读数比例时会考虑基因的长度,因此在分析同一个样本内的基因表达水平时可能会有影响。而TPM在标准化过程中会先对转录本长度进行校正,然后再进行样本间的比较,因此,TPM提供了一种更为统一和可比的表达水平度量。
2.2 TPM标准化在mRNA表达数据分析中的作用
2.2.1 提高数据分析的准确性和可比性
在处理来自不同实验的RNA-Seq数据时,由于样本制备、测序深度等因素的不同,直接比较原始的表达计数通常会导致偏差。TPM标准化提供了一种校正这些变量的方法,通过统一的标准化过程,确保比较的是真正的生物学信号而非技术差异。
2.2.2 TPM标准化对后续分析的影响
标准化后的TPM值可以用于多种下游分析,如差异表达分析、基因功能富集分析等。因为TPM标准化后的数据能够更真实地反映基因的表达水平,因此可以提高这些分析的准确性和可靠性。此外,标准化后的数据还可以用于跨样本或跨实验组的比较,进而揭示生物学上的重要差异。
2.3 实践TPM标准化的案例分析
2.3.1 标准化流程详解
进行TPM标准化的第一步是获取原始计数数据,然后按照以下步骤进行标准化:
- 对于每个样本,计算总转录本计数(百万级)。
- 计算每个基因的转录本计数占总转录本计数的比例。
- 将比例乘以10^6,获得TPM值。
以下是一个简化的示例,展示如何使用Python进行TPM标准化:
import pandas as pd
# 假设我们有原始计数数据存储在CSV文件中,文件名为counts.csv
data = pd.read_csv('counts.csv', index_col=0)
# 计算每个样本的总转录本计数(百万级)
total_counts_per_million = data.sum(axis=0) / 1e6
# 计算TPM
tpm = data.apply(lambda x: (x / total_counts_per_million[x.name]) * 1e6)
print(tpm)
2.3.2 标准化结果的解释和应用
TPM标准化结果可以直接用于后续分析。例如,在差异表达分析中,可以通过比较不同条件下的TPM值来确定哪些基因表达水平有显著差异。在预后预测和生存分析中,TPM值也可以作为输入变量来构建预后模型。
表1展示了标准化前后的数据比较,可以清楚看到标准化后数据在不同样本间具有更高的可比性:
| 基因 | 样本1原始计数 | 样本2原始计数 | 样本1TPM | 样本2TPM |
|---|---|---|---|---|
| GeneA | 1000 | 2000 | 5.3 | 6.4 |
| GeneB | 5000 | 10000 | 26.5 | 32.1 |
通过上述过程,我们能够更好地理解和使用TPM标准化方法,并将其应用于精确的基因表达数据分析中。
3. mRNA表达数据的log2转换及对数尺度分析
3.1 log2转换的基本原理
3.1.1 对数转换的数学背景
在生物学实验数据分析中,尤其是基因表达数据的处理,对数转换是一种常用的数据转换方法。对数转换的数学基础源自对数函数的性质。对数函数能够压缩较大的数值范围,使得大数值之间的差异在对数尺度上变小,而小数值之间的差异则相对放大。这种转换特别有助于处理生物学实验中常见的、数据分布极度偏斜的情况,如基因表达数据通常呈长尾分布。通过对数转换,可以将原始的偏态分布数据转换为近似正态分布,从而满足许多统计分析方法对数据分布的假设。
3.1.2 log2转换在mRNA表达数据中的应用
在mRNA表达数据处理中,常用的方法是对原始表达量进行log2转换。之所以使用log2而不是其他底数的对数,是因为生物学中许多过程,如基因拷贝数的倍增或基因表达的倍数变化,通常是基于2的倍数进行的。例如,某基因在实验条件下表达量翻倍,其表达倍数变化为2。若使用log2表达这个变化,则为1(log2(2) = 1),这直观地反映了表达倍数的变化。log2转换后的表达数据具有以下特点:一是缩小了数据范围,使得后续分析更加稳定;二是可以直观地反映表达量的变化倍数。
3.2 log2转换在数据分析中的重要性
3.2.1 对数尺度的优势和应用场景
对数尺度的一个重要优势是能够使得数据的分布更接近正态分布,从而使得一些依赖于数据正态性的统计分析方法可以应用于原本非正态分布的数据。在基因表达分析中,这一优势尤为重要,因为它使得我们能够使用如t检验或ANOVA等检验方法,这些方法在原始的非对数尺度数据上可能不适用。应用场景广泛,包括差异表达基因的识别、聚类分析、主成分分析等。在这些应用场景中,log2转换可以帮助平滑数据,减少异常值的影响,从而提高分析结果的可靠性和准确性。
3.2.2 对数尺度对数据分析的影响
对数转换的一个关键影响是对差异表达基因分析的影响。例如,考虑两个样本中某个基因的表达量分别为2和8,那么在对数尺度上(log2尺度),这个基因的表达变化量为3(log2(8) - log2(2) = 3 - 1 = 2)。这表明该基因在这两个样本中的表达量相差2倍。在实际数据分析中,使用log2转换可以帮助我们更直观地判断基因表达量的变化倍数,并且在进行差异表达分析时,对数尺度上的均值和方差能够更加稳定,进而使得统计检验更加有效。
3.3 log2转换的数据处理和分析实践
3.3.1 log2转换的具体步骤
在实际操作中,对mRNA表达数据进行log2转换通常涉及以下步骤:
- 读取原始的表达矩阵数据,通常是一个包含多个样本和基因的表格。
- 使用适当的编程语言或软件工具(如R语言的
log2()函数)对每个表达值进行log2转换。 - 处理数据中的零值,通常通过加1或其他小常数来避免对数值无穷大或未定义的情况。
- 转换后的数据存储在新的矩阵中,用于后续分析。
以下是一个简单的R代码示例,展示了如何对数据集进行log2转换:
# 假设原始的表达数据集名为expression_matrix
expression_matrix <- read.csv("expression_data.csv")
# 对原始数据集中的每个值应用log2转换
log2_expression_matrix <- log2(expression_matrix + 1)
# 将转换后的数据集保存为新的文件
write.csv(log2_expression_matrix, "log2_expression_data.csv")
在上述代码中, expression_matrix 为原始表达矩阵, +1 是为零值添加的一个小常数,以避免对数值无穷大或未定义的情况,最后将转换后的数据集保存为新的CSV文件。
3.3.2 转换后的数据处理和分析策略
一旦数据经过log2转换,就可以进行各种后续的统计分析和可视化了。在差异表达分析中,可以应用t检验、limma包中的voom函数或DESeq2等工具,对不同组间的基因表达差异进行统计测试。可视化手段,如箱线图、散点图或热图,可以帮助直观地展示log2转换后的数据特征及其分布情况。在进行这些分析时,需注意以下策略:
- 数据的正态性和方差齐性检验 :尽管log2转换有助于满足正态性和方差齐性的统计假设,但在进行统计测试前,仍应检验这些假设是否满足。
- 异常值的处理 :尽管对数转换减少了异常值的影响,但在异常值较多的情况下,仍然需要考虑是否进行适当的数据清洗。
- 样本大小和实验设计 :确保样本大小足够,并且实验设计反映了研究目的,这对于后续分析的有效性至关重要。
通过实施上述策略,研究者可以充分利用log2转换带来的数据处理优势,进行深入而精确的生物信息学分析。
4. 差异表达分析与富集分析的方法
4.1 差异表达分析的基本流程
4.1.1 差异表达分析的目的和方法
差异表达分析是基因表达研究中的核心步骤,其目的在于识别在不同条件或组别中表达水平存在显著差异的基因。这些差异可能反映了生物学过程中的关键变化,例如疾病状态与正常状态的对比,或治疗组与对照组的对比。识别出的差异表达基因(DEGs)是后续功能注释、通路分析和生物标志物发现等研究的基础。
差异表达分析的方法多种多样,常见的有t检验、ANOVA(方差分析)、LIMMA(线性模型的微阵列分析)以及基于负二项分布的边缘检验等。每种方法都有其特定的适用条件和统计假设。例如,t检验适用于两组数据的比较,而ANOVA可以扩展到多组数据的比较。LIMMA是一种结合了线性模型和经验贝叶斯方法的工具,适合处理微阵列数据,并且在样本量较少时仍具有较高的统计功效。负二项检验则适用于处理计数数据,特别是当数据具有过度离散(over-dispersion)问题时。
4.1.2 差异表达分析的统计学基础
差异表达分析的统计学基础是假设检验,目的是评估不同样本群体之间表达水平的差异是否具有统计学意义。在差异表达分析中,通常会先假设两组之间没有表达差异,即零假设(H0)。通过计算p值来决定是否拒绝零假设。p值是指在零假设为真的条件下,观察到当前数据或更极端情况出现的概率。如果p值小于预设的显著性水平(如0.05),则拒绝零假设,认为存在统计学上的差异表达。
除了p值,差异表达分析还需要考虑多重假设检验的问题。在分析成千上万的基因表达时,即使在没有生物学差异的情况下,也有可能偶然得到一些显著的p值。因此,通常会应用校正方法(如Benjamini-Hochberg方法)来控制假阳性率(False Discovery Rate, FDR)。
4.2 差异表达分析的实践操作
4.2.1 差异表达基因的识别和分类
差异表达基因的识别过程通常涉及以下步骤:
- 数据预处理:包括标准化、归一化等步骤,以消除非生物学变异带来的影响。
- 应用适当的统计检验方法对基因表达数据进行分析,得到基因的p值和效应大小(如log2 Fold Change)。
- 应用多重假设检验校正方法,比如Benjamini-Hochberg方法来计算校正后的p值或FDR。
分类差异表达基因通常基于差异表达的统计显著性(校正后的p值)以及表达变化的大小(如log2 Fold Change的绝对值)。常用的分类标准如下:
- 显著上调(上调基因):具有显著的小于零的log2 Fold Change值和小于预设显著性水平的校正p值。
- 显著下调(下调基因):具有显著的大于零的log2 Fold Change值和小于预设显著性水平的校正p值。
- 非显著表达差异:不满足上述标准的基因。
4.2.2 差异表达分析的结果解释
差异表达基因的分析结果需要结合生物学背景进行解释。这通常包括:
- 对于识别出的基因,评估它们在已知的生物学通路、网络和功能中的角色。
- 利用公共数据库和文献资源验证这些基因是否与特定的生物过程或疾病状态相关联。
- 将差异表达基因作为候选者,进行进一步的实验验证和功能研究。
在解释结果时,需要注意以下几点:
- 统计显著性并不总是等同于生物学意义。一个基因可能表达变化非常显著,但如果其表达水平非常低,那么其生物学意义可能有限。
- 需要考虑实验设计和生物学重复的充分性。样本量太小或缺乏生物学重复可能会导致结果不可靠。
- 应避免单一数据源的偏见,应利用多个数据源或数据库验证发现,以增强发现的可信度。
4.3 富集分析的策略与应用
4.3.1 富集分析的目的和原理
富集分析(Enrichment Analysis)是一种用来识别在差异表达基因中过度代表的特定基因集(如通路、功能分类、基因本体)的方法。它基于这样的假设:如果一系列基因在某些生物学过程中起着关键作用,那么这些基因在差异表达基因列表中出现的频率将高于在全部基因列表中的频率。
富集分析的常用方法包括基因本体(Gene Ontology, GO)富集分析和通路富集分析(如KEGG通路分析)。这些方法依赖于基因功能注释和预先定义的基因集合。
4.3.2 富集分析在研究中的实例应用
以下是进行GO富集分析的一个简化的实例步骤:
- 从差异表达分析中选取显著上调或下调的基因列表。
- 利用GO注释数据库,获取与这些基因相关的GO术语。
- 应用富集分析算法(如Hypergeometric test)计算每个GO术语的富集p值。
- 应用多重假设检验校正方法,得到校正后的p值或FDR。
- 根据校正后的p值和/或Fold Change,筛选出显著富集的GO术语。
- 分析和解读富集结果,识别关键的生物学过程、分子功能和细胞组分。
富集分析结果通常以图表形式展示,例如柱状图和气泡图可以直观显示富集显著的GO术语。表格列出具体的基因列表和相应的富集统计结果。
在解释富集分析结果时,研究者需要关注以下方面:
- 富集分析结果需要结合实验的生物学背景进行解读,不是所有富集的GO术语都一定具有实际生物学意义。
- 富集结果可以帮助研究者识别出可能的生物学通路和过程,但需要进一步实验验证。
- 结合差异表达分析和富集分析结果,研究者可以构建更加全面的生物学假设,并设计相应的功能验证实验。
通过本章节的介绍,我们已经深入理解了差异表达分析和富集分析的理论基础和实践操作,及其在基因表达研究中的重要性和应用。这些分析方法为研究者提供了一种强有力的工具来揭示生物样本之间基因表达模式的差异,为进一步的生物信息学分析和实验验证奠定了基础。
5. 结合临床信息的生存分析和预后预测
5.1 生存分析的统计学基础
生存分析是专门用来处理生存时间数据的统计方法,它广泛应用于医学、生物学和其他领域,用以研究和预测不同条件下个体的生存情况。生存时间可以是发生某种事件(如疾病的复发或患者的死亡)所需的时间。
5.1.1 生存分析的定义和类型
生存分析的核心是生存函数,它表示一个群体中生存时间超过某一特定值的概率。生存分析的类型主要包括:
- 无条件生存分析 :不考虑任何协变量的情况,一般用于描述总体的生存趋势。
- 条件生存分析 :考虑协变量的存在,研究在特定条件下(如某次治疗后)的生存情况。
5.1.2 生存时间数据的处理方法
生存时间数据的分析常常涉及以下方法:
- Kaplan-Meier曲线 :非参数估计方法,用于估计生存函数,适用于处理右删失数据(即只知道生存时间大于某个值的情况)。
- Cox比例风险模型 :半参数模型,用于分析影响生存时间的协变量,并评估这些因素的风险比。
5.2 生存分析在临床数据中的应用
在临床数据中,生存分析通常用于评估治疗方案的效果、预测患者预后以及识别对生存时间有显著影响的临床因素。
5.2.1 生存曲线的绘制和解读
通过绘制生存曲线,可以直观地展示不同组别或条件下的生存趋势。生存曲线的交叉、分离或重叠都能够提供有关生存时间分布的重要信息。
- 曲线交叉 :表明不同组别的生存函数随时间的变化趋势发生变化,可能需要进一步的比较检验。
- 曲线分离 :表示一组的生存概率始终高于另一组,反映出影响生存时间的显著因素。
- 曲线重叠 :可能意味着生存时间在统计上没有显著差异。
5.2.2 影响生存时间的临床因素分析
在临床数据中,识别影响生存时间的因素是至关重要的。这些因素可能包括:
- 年龄
- 性别
- 病理阶段
- 治疗方案
通过生存分析方法,可以评估这些因素对生存时间的独立影响,并通过风险比来量化其影响程度。
5.3 预后预测的构建与验证
预后预测模型是基于临床和生物标志物信息,对患者预后进行评估的工具。预后模型的构建和验证是生存分析中的重要步骤。
5.3.1 预后模型的构建方法
构建预后模型通常包括以下步骤:
- 变量选择 :通过单变量和多变量分析,选择对生存时间有显著影响的变量。
- 模型建立 :使用Cox比例风险模型或其它回归模型构建预后预测模型。
- 模型检验 :通过交叉验证、Hosmer-Lemeshow检验等方法检验模型的预测能力。
5.3.2 预后预测的评估和应用实例
预后预测模型的评估包括:
- 区分度 :模型对高风险和低风险患者区分的能力。
- 校准度 :预测值与实际发生情况的一致性。
应用实例可能涉及到具体的临床试验或研究,展示如何利用预后预测模型指导临床决策和治疗选择。以下是预后预测模型在临床实践中的一个示例应用:
- 示例应用 :假设研究者开发了一个基于患者年龄、肿瘤大小和癌细胞分化程度的预后预测模型。通过收集TCGA-KIRC数据集中的临床信息,研究者可能发现,对于肾脏透明细胞癌患者,该模型能够显著区分生存时间的长短,并且模型预测与实际生存情况高度一致,从而为个体化治疗提供了有力的工具。
通过第五章的介绍,我们已经了解了生存分析和预后预测的基本概念、方法以及在临床信息分析中的重要应用。在实际应用中,这些分析能够极大地辅助临床决策,提高患者的生存质量。
简介:TCGA是一项国际癌症研究项目,专注于通过基因组和转录组分析提升癌症理解。TCGA-KIRC研究专项针对肾透明细胞癌,提供了标准化mRNA表达数据(TPM格式)及临床信息。数据集可用于分析基因表达变化、寻找疾病相关基因,并结合临床特征探索基因与临床结果之间的关联。数据处理步骤包括清洗、转换、统计分析及生存分析,有助于揭示疾病的分子机制并推动新疗法发展。

DAMO开发者矩阵,由阿里巴巴达摩院和中国互联网协会联合发起,致力于探讨最前沿的技术趋势与应用成果,搭建高质量的交流与分享平台,推动技术创新与产业应用链接,围绕“人工智能与新型计算”构建开放共享的开发者生态。
更多推荐
 已为社区贡献7条内容
已为社区贡献7条内容







所有评论(0)